Zakon stalnih odnosa masa- Test za 7. razred
1. U kojim masenim odnosima se jedine ugljenik i kiseonik pri građenju ugljen-dioksida?

2. Da li se za reakciju troši celokupna količina kiseonika ukoliko se zapali 3g magnezijuma u sudu u kome se nalazi 5g kiseonika?
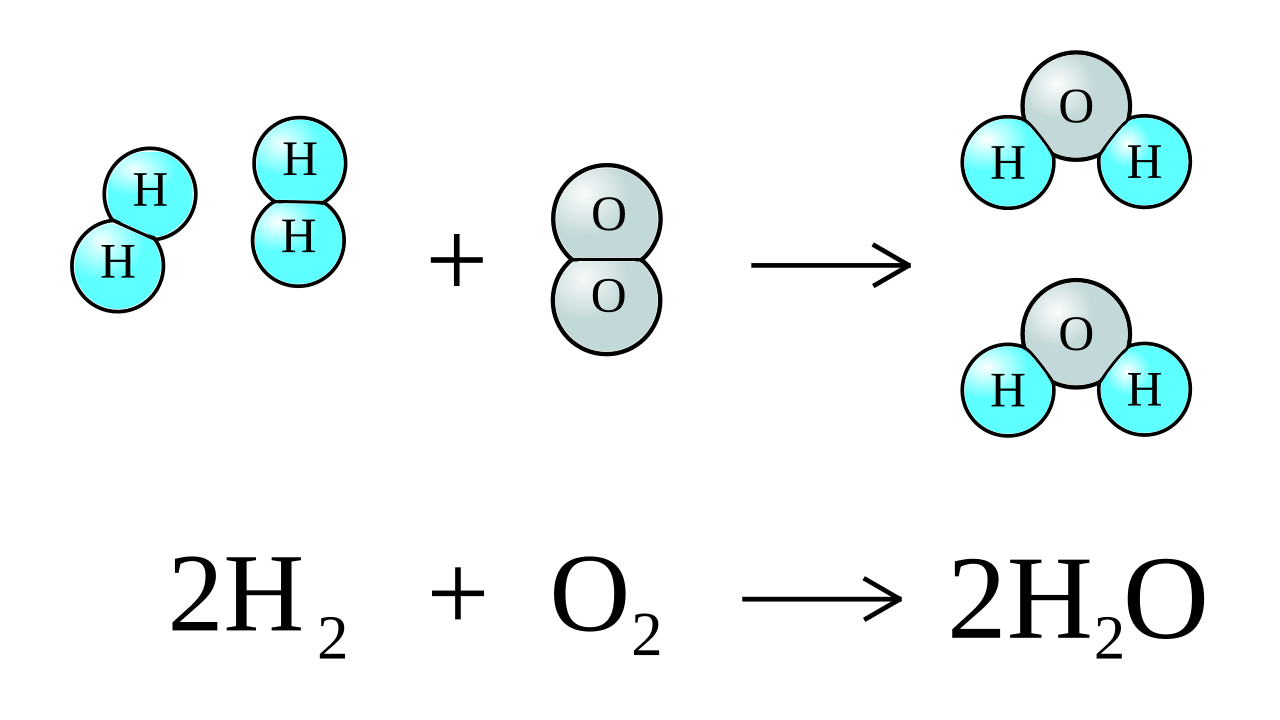
3. Maseni odnos vodonika i kiseonika pri građenju molekula vode je:

4. Zakon stalnih odnosa masa podrazumeva da:
5. Pomoću zakona stalnih odnosa masa elemenata u jedinjenju možemo odrediti:
6. Kako glasi zakon o održanju mase?

7. Zakon stalnih odnosa masa je definisao:
8. Po kojoj formuli izračunavamo maseni udeo elemenata u jedinjenju?

9. Odnos masa sumpora i kiseonika u jedinjenju je 1:1. Koja je formula tog jedinjenja?

10. Molekul vode se uvek sastoji od jednog atoma kiseonika i dva atoma vodonika.
11. Relativna molekulska masa jednog oksida je 44, a odnos masa azota i kiseonika 7:4. Koja je formula tog oksida azota?

12. Ugljen(IV)-oksid nastaje potpunim sagorevanjem ćumura i razlaganjem krečnjaka dejstvom visoke temperature. U prvom slučaju ugljen(IV)-oksid sadrži 1 atom ugljenika, a 2 atoma kiseonika, dok je u drugom sastavljen od 2 ugljenikova atoma i 2 kiseonikova atoma.
ШТА ЖЕЛИШ ДА УРАДИШ?
ВИДИ РЕЗУЛТАТЕ
ПОШАЉИ РЕЗУЛТАТЕ
Резултат теста



